Estima-se que o suíno tenha um total de 1010-1012 bactérias no intestino, um número dez vezes maior que o total de células do seu corpo (Luckey, 1972). É essencial que este componente bacteriano seja tido em conta ao conceber as dietas para os animais, porque através de uma microbiota mais saudável e mais favorável para o suíno, podemos influenciar diretamente o processo de digestão mais eficiente, melhorando o sistema imune e aumentando o rendimento produtivo.
A influência sobre a microbiota pode ser exercida das seguintes formas:

Modificando a disponibilidade de nutrientes para determinadas espécies bacterianas
Em geral, as bactérias do cólon proximal têm uma grande contribuição de nutrientes, provenientes de resíduos não digeridos da dieta na seção do intestino delgado, que vão se reduzindo e limitando à medida que se vão alcançando as regiões distais.
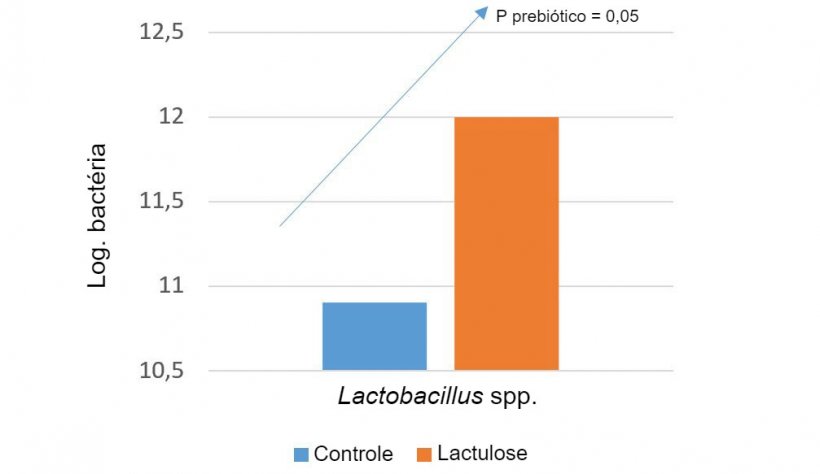
Uma das estratégias para influenciar nesse aspecto são os prebióticos. O conceito de prebióticos começou quando foi observado que a inulina e os fruto-oligossacáridos (FOS) estimulavam as bifidobactérias, consideradas boas para a saúde intestinal (Gibson e Roberfroid, 1995). Atualmente existe muita literatura em suínos que suporta o uso de prebióticos para selecionar Bifidobacterium spp., Lactobacillus spp., Bacteroides spp., etc. Atribui-se também essa capacidade de influenciar a microbiota à inclusão, na dieta, de um determinado nível de fibra fermentável, para estimular a fermentação do cólon (Correa-Matos, 2003), a redução dos níveis de proteína na dieta, para evitar a fermentação proteica (Pérez, 2013) e à inclusão de enzimas exógenas, quando da produção de oligossacáridos com efeito prebiótico a partir de polissacáridos não-amiláceos (Bedford, 2004).
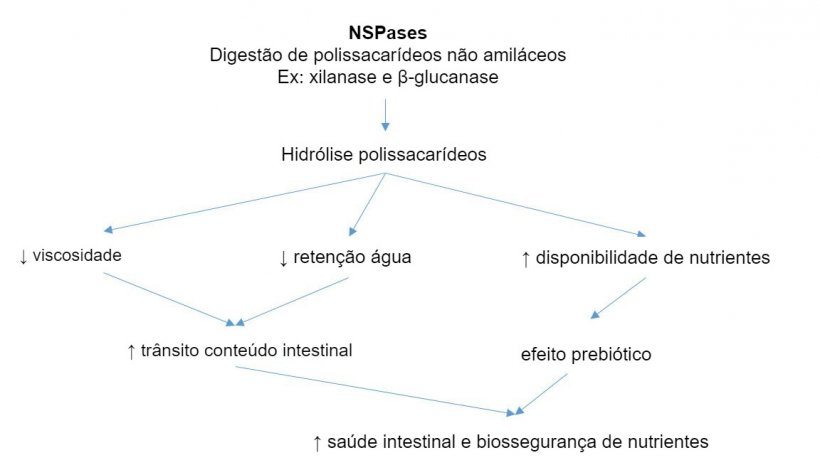
Por sua vez, também se pode planejar um tratamento probiótico com o objetivo de modificar os nutrientes presentes no intestino. Para começar, pode ser desenhada uma estratégia para reduzir nutrientes específicos e comprometer o crescimento de bactérias patogênicas, fomentando uma população mais favorável para os suínos. Esses objetivos são alcançados através do uso de bactérias probióticas que competem por esses nutrientes e os utilizam de maneira mais eficiente (Gerritsen et al., 2011). Por outro lado, outras estratégias probióticas baseiam-se na alimentação cruzada, que consiste em fornecer um probiótico que fornece produtos metabólicos específicos para promover as bactérias que mais interessam. Um exemplo dessa prática seria o estudo de Belenguer et al. (2006) onde, através da produção de lactato e acetato por bifidobactérias, estimulavam o crescimento de outras bactérias butirogênicas (fornecendo energia para os colonócitos).
Provocando mudanças no meio
As mudanças no ambiente fermentativo e no pH também influenciam o perfil da microbiota. Isto pode ser conseguido diretamente com acidificantes ou, indiretamente, com probióticos, por exemplo, com bactérias ácido-lácticas, que produzem ácido lático como um metabólito principal (Yang et al., 2015). A fermentação de prebióticos, como FOS ou inulina, também leva à produção de ácidos orgânicos, que reduzem o pH intestinal e dificultam a colonização por enterobactérias ou clostrídios sensíveis a este pH ácido.
Interferindo na comunicação bacteriana (Quorum Sensing)
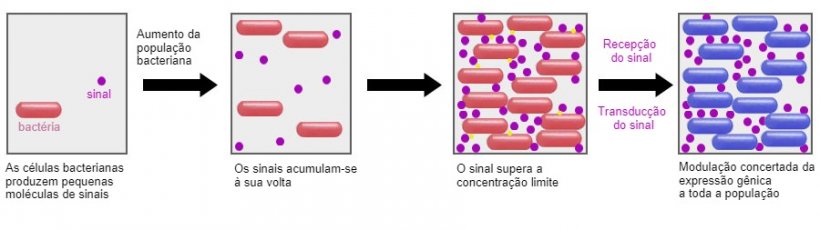
Uma linha de pesquisa muito promissora é interferir no Quorum Sensing (QS), o mecanismo de comunicação entre as bactérias. Essa comunicação é feita através de moléculas sinalizadoras e permite que se crie uma resposta coordenada, ativando ou desativando a expressão de determinados genes e, eventualmente, atuando como um coletivo, proporcionando vantagens de sobrevivência como a formação de biofilmes ou esporulação (Hughes e Sperandio, 2008). ). Através do uso de probióticos específicos, que liberam outras moléculas sinalizadoras, ou, na falta desta, enzimas que hidrolisam as moléculas sinalizadoras presentes, podemos afetar essas vias de QS (Brown, 2011). No entanto, deve ser mencionado que grande parte da informação que atualmente temos disponível sobre a comunicação bacteriana está no nível in vitro, e será interessante ver se os resultados dos testes in vivo são consistentes ou dependem do ambiente gastrointestinal do animal.
Modificando os padrões de colonização e desenvolvimento do trato gastrointestinal

Finalmente, vale a pena notar que as primeiras semanas de vida são um estágio em que todas essas estratégias serão potencialmente muito mais eficazes e duradouras. Por um lado, foi descrito que a microbiota neonatal é relativamente dinâmica e muito influenciada pelo ambiente e pela microbiota materna. Por outro lado, a composição microbiana neste estágio é determinante para o futuro, fato conhecido como "microbial imprinting " (Konstantinov et al., 2006). Por sua vez, sabe-se também que a microbiota desempenha um papel essencial na educação do trato gastrointestinal imaturo para gerar sistemas funcionalmente eficientes quando o animal for adulto (Lewis et al., 2012). Isso é evidente em estudos com animais germ-free, onde foi descrito que animais sem microbiota têm sistema imunológico e arquitetura intestinal sub-desenvolvidos (Luczynski et al., 2016). Isso mesmo foi demonstrado em estudos em granjas, onde animais expostos a maior diversidade microbiana desde o nascimento têm sido associados a um perfil microbiano mais saudável, adaptável a mudanças ambientais e mais resistentes a bactérias potencialmente perigosas (Mulder et al., 2009). Em conclusão, do ponto de vista prático, a etapa neonatal, e mesmo as porcas reprodutoras, podem ser os momentos mais eficazes para influenciar a microbiota, estabelecendo benefícios mais robustos e duradouros (Kenny et al., 2011).



