O que é edição genética?
A edição genética permite que mudanças precisas sejam feitas no genoma dos organismos. Isso significa fazer modificações adicionando, alterando ou excluindo com precisão pares de bases nitrogenadas da sequência de DNA. Dentre todas as técnicas disponíveis, a tecnologia CRISPR-Cas9 ganhou grande popularidade devido à sua alta eficiência, precisão e relativa simplicidade de uso.
Como funciona o CRISPR-Cas9?
- É usado um RNA guia, que é uma pequena sequência de 20 pares de bases que corresponde à parte do DNA que você deseja modificar.
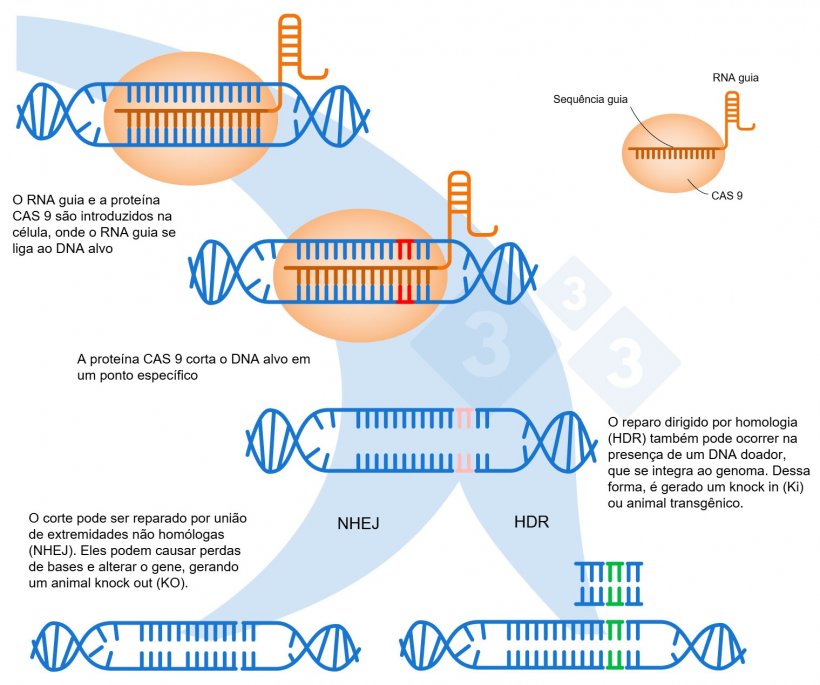
- Esse guia leva a enzima Cas9 exatamente ao local onde deve ser feito o corte nas duas fitas de DNA (Figura 1).
- Após o corte, o organismo tenta reparar o DNA por meio de um processo denominado junção de extremidades não homólogas (NHEJ). Durante este reparo, alguns pares de bases podem ser adicionados ou perdidos no local do corte.
- Essas alterações no DNA podem alterar o quadro de leitura do gene, causando alterações na sequência de aminoácidos da proteína produzida pelo gene. Como resultado, a proteína pode ficar defeituosa ou para de funcionar completamente (Figura 2).
|
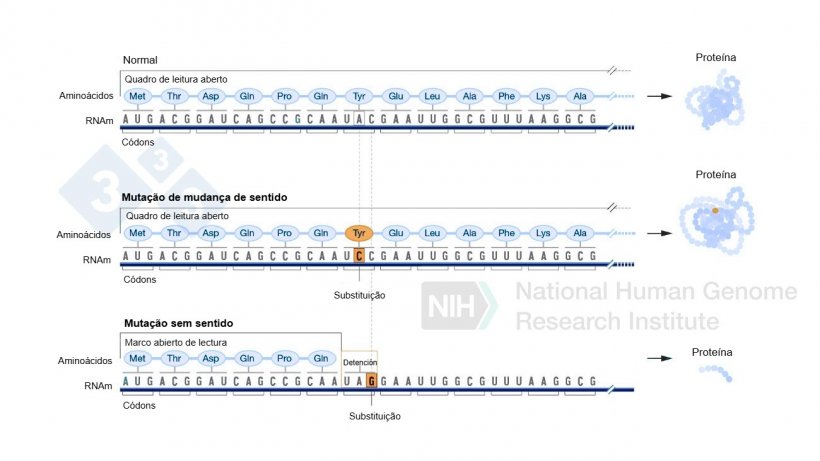
Lembremos que as proteínas são constituídas por longas cadeias de aminoácidos, que são as unidades básicas das proteínas. Existem 20 tipos diferentes de aminoácidos, e cada um deles é codificado por uma sequência específica de três bases nitrogenadas no DNA, conhecidas como tripletos ou códons. Essas bases podem ser adenina, citosina, timina e guanina.  Quando o quadro de leitura do DNA (isto é, a forma como as bases são agrupadas em tripletos) é alterado, a sequência de códons também muda. Isto pode levar à incorporação de aminoácidos incorretos durante a síntese proteica, ou mesmo causar o aparecimento de um códon de parada, que perturba a formação de proteínas. (Figura 2). |

Animais knock-out: quando mudanças no DNA desativam uma proteína
Um animal é considerado knock-out (KO) para um gene específico quando alterações genéticas inativam a função de uma proteína. Essas alterações são semelhantes às mutações que poderiam ocorrer naturalmente por meio de processos espontâneos, mas, neste caso, são realizadas de forma controlada e direcionada. Portanto, não é possível distinguir se uma mutação em um animal ocorreu naturalmente ou foi induzida em laboratório.
|
É importante ressaltar que neste processo NÃO é introduzido material genético de outras espécies, portanto os animais KO gerados por esta técnica não são considerados transgênicos. |
Um exemplo de animal KO são os animais resistentes ao vírus PRRS. Para que o vPPRS infecte o suíno, é necessário que ele se ligue a um receptor específico presente nos macrófagos alveolares dos pulmões do animal. Este receptor é codificado pelo domínio SRCR5 do gene CD163 (Figura 3). Se este receptor for modificado ou eliminado através da edição genética, o vírus já não consegue aderir às células, evitando a infecção e tornando o suíno completamente resistente ao PRRSv. Esta resistência genética pode ser herdada pela descendência, garantindo que as gerações futuras serão resistentes ao PRRS.
Animais Knock-in: Introdução de novas cadeias de DNA e novos genes
Uma alternativa na edição genética consiste em aproveitar o momento em que o DNA é cortado pelo Cas9 para introduzir uma nova fita de DNA. Ao fazer isso, a célula pode incorporar esse novo material genético por meio de um processo denominado recombinação dirigida homóloga (HDR). Isto permite substituir uma sequência de DNA defeituosa por uma funcional e corrigir o gene para que volte a funcionar ou alterar o quadro de leitura para gerar um animal KO, no qual um gene foi desativado. Além disso, essa técnica permite a inserção de um novo gene adicional que não existia antes, no genoma do organismo, conhecido como knock-in (KI) ou transgênico.
| Se o gene introduzido vier de outra espécie, cria-se uma combinação genética que não ocorre naturalmente. Esse tipo de organismo é denominado animal transgênico, pois possui genes de outra espécie integrados em seu DNA. |
Um exemplo de suínos transgênicos seriam aqueles nos quais foi inserido o gene UPC1, que não está naturalmente presente nesta espécie. Este gene permite-lhes regular melhor a temperatura corporal, o que os torna mais adaptados para suportar baixas temperaturas. Como resultado, os suínos acumulam menos gordura subcutânea para manter a temperatura corporal, o que aumenta a percentagem de tecido magro (Figura 3).

Editores de base: uma ferramenta precisa na edição de genes
Uma alternativa mais recente na edição genética é o uso de editores de bases, que são enzimas especializadas que, em vez de cortar o DNA, trocam com precisão um par de bases em um local específico do genoma. Este processo permite que mudanças específicas sejam feitas no DNA sem gerar quebras.
Este tipo de substituição pode ter vários efeitos. Em alguns casos, a alteração introduz um códon de parada, que interrompe prematuramente a produção da proteína, deixando-a incompleta e possivelmente não funcional. Noutros casos, a alteração altera um aminoácido na proteína (conhecida como mutação missense), que pode alterar a sua estrutura e afetar a sua função. Em ambos os casos, estas alterações podem comprometer a funcionalidade da proteína.
Todos os suínos com edição genética são iguais? Regulamento Normativo x Desenvolvimento técnico
É importante compreender tecnicamente os diferentes tipos de edição genética, uma vez que as regulamentações que se aplicam, ou deveriam aplicar, variam em cada caso. Atualmente, a maior parte da legislação mundial limita estritamente o uso de animais transgênicos e a comercialização de seus produtos. No entanto, estão a ser feitos progressos na distinção entre animais geneticamente editados e animais transgênicos, o que poderia levar a regulamentações diferenciadas. Tecnicamente, estes dois tipos de modificações genéticas são totalmente diferentes.

Na União Europeia, os regulamentos relativos a produtos vegetais editados por genes, chamados de novas técnicas genômicas (NGT), já estão a ser revistos. Isto poderia permitir que estas plantas ficassem isentas das leis que regulam as culturas transgênicas chamadas organismos geneticamente modificados (OGM). No entanto, até à data, os animais com genes editados continuam sujeitos à legislação sobre OGM, o que limita o seu desenvolvimento e comercialização futura.
Projeto financiado pela Fundação Seneca 22065/PI/22.


